Nitrogen Oksida
Umum
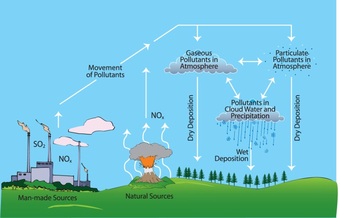
Nitrogen oksida (NOx) adalah senyawa gas yang terdapat di udara bebas (atmosfer) yang sebagian besar terdiri atas nitrit oksida (NO) dan nitrogen dioksida (NO2) serta berbagai jenis oksida dalam jumlah yang lebih sedikit. Kedua macam gas tersebut mempunyai sifat yang sangat berbeda dan keduanya sangat berbahaya bagi kesehatan. Gas NO yang mencemari udara secara visual sulit diamati karena gas tersebut tidak bewarna dan tidak berbau. Sedangkan gas NO2 bila mencemari udara mudah diamati dari baunya yang sangat menyengat dan warnanya merah kecoklatan. Sifat Racun (toksisitas) gas NO2 empat kali lebih kuat dari pada toksisitas gas NO. Organ tubuh yang paling peka terhadap pencemaran gas NO2 adalah paru-paru. Paru-paru yang terkontaminasi oleh gas NO2 akan membengkak sehingga penderita sulit bernafas yang dapat mengakibatkan kematiannya (Fardiaz, 1992).
Kadar NOx di udara daerah perkotaan yang berpenduduk padat akan lebih tinggi dibandingkan di pedesaan karena berbagai macam kegiatan manusia akan menunjang pembentukan NOx, misalnya transportasi, generator pembangkit listrik, pembuangan sampah, dan lain-lain. Namun, pencemar utama NOx berasal dari gas buangan hasil pembakaran bahan bakar gas alam (Wardhana, 2004).
Udara yang mengandung gas NO dalam batas normal relatif aman dan tidak berbahaya, kecuali bila gas NO yang tinggi dapat menyebabkan gangguan pada sisitem saraf yang menyebabkan kejang-kejang. Bila keracunan ini terus berlanjut akan dapat menyebabkan kelumpuhan. Gas NO akan menjadi lebih berbahaya apabila gas itu teroksidasi oleh oksigen sehingga menjadi gas NO2. Di udara nitrogen monoksida (NO) teroksidasi sangat cepat membentuk nitrogen dioksida (NO2) yang pada akhirnya nitrogen dioksida (NO2) teroksidasi secara fotokimia menjadi nitrat (Sastrawijaya, Tresna. 1991).
Kadar NOx di udara daerah perkotaan yang berpenduduk padat akan lebih tinggi dibandingkan di pedesaan karena berbagai macam kegiatan manusia akan menunjang pembentukan NOx, misalnya transportasi, generator pembangkit listrik, pembuangan sampah, dan lain-lain. Namun, pencemar utama NOx berasal dari gas buangan hasil pembakaran bahan bakar gas alam (Wardhana, 2004).
Udara yang mengandung gas NO dalam batas normal relatif aman dan tidak berbahaya, kecuali bila gas NO yang tinggi dapat menyebabkan gangguan pada sisitem saraf yang menyebabkan kejang-kejang. Bila keracunan ini terus berlanjut akan dapat menyebabkan kelumpuhan. Gas NO akan menjadi lebih berbahaya apabila gas itu teroksidasi oleh oksigen sehingga menjadi gas NO2. Di udara nitrogen monoksida (NO) teroksidasi sangat cepat membentuk nitrogen dioksida (NO2) yang pada akhirnya nitrogen dioksida (NO2) teroksidasi secara fotokimia menjadi nitrat (Sastrawijaya, Tresna. 1991).
Karakteristik
Nitrogen oksida dapat merujuk pada senyawa biner oksigen dan nitrogen, atau campuran senyawa-senyawa berikut:
Keberadaan NOx di udara dapat dipengaruhi oleh sinar matahari yang mengikuti daur reaksi fotolitik NO2 sebagai berikut :
- Nitrat oksida, juga dikenal sebagai nitrogen monoksida, (NO), nitrogen (II) oksida
- Nitrogen dioksida (NO2), nitrogen (IV) oksida
- Nitrat oksida (N2O), nitrogen (-I, III) oksida
- Nitrosylazide (N4O), nitrogen (-I, 0, I, II) oksida
- Nitrat radikal (NO3), nitrogen (VI) oksida
- Dinitrogen trioksida (N2O3), nitrogen (II, IV) oksida
- Dinitrogen tetroksida (N2O4), nitrogen (IV) oksida
- Dinitrogen pentoksida (N2O5), nitrogen (V) oksida
- Trinitramide (N(NO2)3), nitrogen (0, IV) oksida
Keberadaan NOx di udara dapat dipengaruhi oleh sinar matahari yang mengikuti daur reaksi fotolitik NO2 sebagai berikut :
NO2 + sinar matahari → NO + O
O + O2 → O3 (ozon)
O3 + NO → NO2 + O2
O + O2 → O3 (ozon)
O3 + NO → NO2 + O2
Gas Nitrogen dioksida dengan rumus molekul NO 2 merupakan gas berwarna coklat kemerahan berbau tajam menyengat dan sangat beracun. Memiliki Massa Rumus 46,0055, massa jenis 0,0034 gr/ml, Volume Molar 22,393 liter. Nitrogen dioksida biasanya terbentuk melalui oksidasi oleh oksigen di udara:
2NO + O2 → 2NO2
Di laboratorium, NO2 dapat dibuat dengan cara pentoksida dinitrogen, yang diperoleh melalui dehidrasi asam nitrat:
2 HNO3 → N2O5 + H2O
2 N2O 5 → 4 NO2 + O2
Dekomposisi termal logam beberapa nitrat juga mampu menghasilkan gas NO
2 Pb(NO3)2 → 2PbO + 4NO2 + O2
Reduksi asam nitrat oleh logam (seperti tembaga).
4 HNO3 + Cu → Cu(NO3)2 + 2NO2 +2H2O
Sumber utama NO2 pada atmosfer adalah dari kendaraan di jalan lalu lintas. Sumber utama lainnya adalah dari pembangkit tenaga listrik, pabrik pemanas, dan proses industri. Oksida Nitrogen (NOx) adalah kelompok gas nitrogen yang terdapat di atmosfir yang terdiri dari nitrogen monoksida (NO) dan nitrogen dioksida (NO2). Walaupun ada bentuk oksida nitrogen lainnya, tetapi kedua gas tersebut yang paling banyak diketahui sebagai bahan pencemar udara. Nitrogen monoksida merupakan gas yang tidak berwarna dan tidak berbau sebaliknya nitrogen dioksida berwarna coklat kemerahan dan berbau tajam. Nitrogen monoksida terdapat diudara dalam jumlah lebih besar daripada NO2. Pembentukan NO dan NO2 merupakan reaksi antara nitrogen dan oksigen diudara sehingga membentuk NO, yang bereaksi lebih lanjut dengan lebih banyak oksigen membentuk NO2.
Untuk menentukan konsentrasi gas NOx di udara telah di lakukan dengan menggunakan peralatan spektroskopi analitik yang bekerja berdasarkan serapan inframerah, spektroskopi resonansi ion, kromatografi gas spektroskopi massa. Spektroskopi analitik yang bekerja berdasarkan serapan inframerah peralatan tersebut sangat mahal, tidak dapat digunakan langsung dilapangan, dan diperlukan waktu yang lama untuk mengetahui konsentrasi gas NOx (Miura et al., 1994). Spektroskopi resonansi ion telah digunakan namun tidak akurat dalam analisis kuantitatif, kromatografi gas spektroskopi massa juga digunakan untuk mendeteksi gas NOx di udara namun han ya dapat digunakan pada temperatur yang rendah (Szabo et al., 2003). Metode lain yang dapat digunakan untuk mendeteksi NOx di udara adalah dengan elektro analisis dengan mengembangkan sensor semikonduktor metode yang merupakan alternatif metode yang efektif dan efisien.
2NO + O2 → 2NO2
Di laboratorium, NO2 dapat dibuat dengan cara pentoksida dinitrogen, yang diperoleh melalui dehidrasi asam nitrat:
2 HNO3 → N2O5 + H2O
2 N2O 5 → 4 NO2 + O2
Dekomposisi termal logam beberapa nitrat juga mampu menghasilkan gas NO
2 Pb(NO3)2 → 2PbO + 4NO2 + O2
Reduksi asam nitrat oleh logam (seperti tembaga).
4 HNO3 + Cu → Cu(NO3)2 + 2NO2 +2H2O
Sumber utama NO2 pada atmosfer adalah dari kendaraan di jalan lalu lintas. Sumber utama lainnya adalah dari pembangkit tenaga listrik, pabrik pemanas, dan proses industri. Oksida Nitrogen (NOx) adalah kelompok gas nitrogen yang terdapat di atmosfir yang terdiri dari nitrogen monoksida (NO) dan nitrogen dioksida (NO2). Walaupun ada bentuk oksida nitrogen lainnya, tetapi kedua gas tersebut yang paling banyak diketahui sebagai bahan pencemar udara. Nitrogen monoksida merupakan gas yang tidak berwarna dan tidak berbau sebaliknya nitrogen dioksida berwarna coklat kemerahan dan berbau tajam. Nitrogen monoksida terdapat diudara dalam jumlah lebih besar daripada NO2. Pembentukan NO dan NO2 merupakan reaksi antara nitrogen dan oksigen diudara sehingga membentuk NO, yang bereaksi lebih lanjut dengan lebih banyak oksigen membentuk NO2.
Untuk menentukan konsentrasi gas NOx di udara telah di lakukan dengan menggunakan peralatan spektroskopi analitik yang bekerja berdasarkan serapan inframerah, spektroskopi resonansi ion, kromatografi gas spektroskopi massa. Spektroskopi analitik yang bekerja berdasarkan serapan inframerah peralatan tersebut sangat mahal, tidak dapat digunakan langsung dilapangan, dan diperlukan waktu yang lama untuk mengetahui konsentrasi gas NOx (Miura et al., 1994). Spektroskopi resonansi ion telah digunakan namun tidak akurat dalam analisis kuantitatif, kromatografi gas spektroskopi massa juga digunakan untuk mendeteksi gas NOx di udara namun han ya dapat digunakan pada temperatur yang rendah (Szabo et al., 2003). Metode lain yang dapat digunakan untuk mendeteksi NOx di udara adalah dengan elektro analisis dengan mengembangkan sensor semikonduktor metode yang merupakan alternatif metode yang efektif dan efisien.
Sumber
Dari seluruh jumlah oksigen nitrogen ( NOx ) yang dibebaskan ke udara, jumlah yang terbanyak adalah dalam bentuk NO yang diproduksi oleh aktivitas bakteri. Akan tetapi pencemaran NO dari sumber alami ini tidak merupakan masalah karena tersebar secara merata sehingga jumlah nya menjadi kecil. Yang menjadi masalah adalah pencemaran NO yang diproduksi oleh kegiatan manusia karena jumlahnya akan meningkat pada tempat-tempat tertentu. Kadar NOx diudara perkotaan biasanya 10–100 kali lebih tinggi dari pada di udara pedesaan. Kadar NOx diudara daerah perkotaan dapat mencapai 0,5 ppm (500 ppb). Seperti halnya CO, emisi NOx dipengaruhi oleh kepadatan penduduk karena sumber utama NOx yang diproduksi manusia adalah dari pembakaran dan kebanyakan pembakaran disebabkan oleh kendaraan bermotor, produksi energi dan pembuangan sampah. Sebagian besar emisi NOx buatan manusia berasal dari pembakaran arang, minyak, gas, dan bensin(Pertamina, 2011).
Kadar NOx di udara dalam suatu kota bervariasi sepanjang hari tergantung dari intensitas sinar mataharia dan aktivitas kendaraan bermotor. Perubahan kadar NOx berlangsung sebagai berikut ((Wardhana, 2004):
Kadar NOx di udara dalam suatu kota bervariasi sepanjang hari tergantung dari intensitas sinar mataharia dan aktivitas kendaraan bermotor. Perubahan kadar NOx berlangsung sebagai berikut ((Wardhana, 2004):
- Sebelum matahari terbit, kadar NO dan NO2 tetap stabil dengan kadar sedikit lebih tinggi dari kadar minimum sehari-hari.
- Setelah aktivitas manusia meningkat ( jam 6-8 pagi ) kadar NO meningkat terutama karena meningkatnya aktivitas lalu lintas yaitu kendaraan bermotor. Kadar NO tetinggi pada saat ini dapat mencapai 1-2 ppm.
- Dengan terbitnya sinar matahari yang memancarkan sinar ultra violet kadar NO2 (sekunder) kadar NO2 pada saat ini dapat mencapai 0,5 ppm.
- Kadar ozon meningkat dengan menurunnya kadar NO sampai 0,1 ppm.
- Jika intensitas sinar matahari menurun pada sore hari ( jam 5-8 malam ) kadar NO meningkat kembali.
- Energi matahari tidak mengubah NO menjadi NO2 (melalui reaksi hidrokarbon) tetapi O3 yang terkumpul sepanjang hari akan bereaksi dengan NO. Akibatnya terjadi kenaikan kadar NO2 dan penurunan kadar O3.
Dampak
1. Kesehatan
Oksida nitrogen seperti NO dan NO2 berbahaya bagi manusia. Penelitian menunjukkan bahwa NO2 empat kali lebih beracun daripada NO. Selama ini belum pernah dilaporkan terjadinya keracunan NO yang mengakibatkan kematian. Diudara ambient yang normal, NO dapat mengalami oksidasi menjadi NO2 yang bersifat racun. Penelitian terhadap hewan percobaan yang dipajankan NO dengan dosis yang sangat tinggi, memperlihatkan gejala kelumpuhan sistem syarat dan kekejangan. Penelitian lain menunjukkan bahwa tikus yang dipajan NO sampai 2500 ppm akan hilang kesadarannya setelah 6-7 menit, tetapi jika kemudian diberi udara segar akan sembuh kembali setelah 4–6 menit. Tetapi jika pemajanan NO pada kadar tersebut berlangsung selama 12 menit, pengaruhnya tidak dapat dihilangkan kembali, dan semua tikus yang diuji akan mati. NO2 bersifat racun terutama terhadap paru. Kadar NO2 yang lebih tinggi dari 100 ppm dapat mematikan sebagian besar binatang percobaan dan 90% dari kematian tersebut disebabkan oleh gejala pembengkakan paru (edema pulmonari). Kadar NO2 sebesar 800 ppm akan mengakibatkan 100% kematian pada binatang-binatang yang diuji dalam waktu 29 menit atau kurang. Pemajanan NO2 dengan kadar 5 ppm selama 10 menit terhadap manusia mengakibatkan kesulitan dalam bernapas (Darmono, 2006).
2. Lingkungan
Proses oksidasi di atmosfer mengakibatkan gas-gas tersebut berubah menjadi H2SO4 dan HNO3 meningkatkan keasaman air hujan.
Oksida nitrogen seperti NO dan NO2 berbahaya bagi manusia. Penelitian menunjukkan bahwa NO2 empat kali lebih beracun daripada NO. Selama ini belum pernah dilaporkan terjadinya keracunan NO yang mengakibatkan kematian. Diudara ambient yang normal, NO dapat mengalami oksidasi menjadi NO2 yang bersifat racun. Penelitian terhadap hewan percobaan yang dipajankan NO dengan dosis yang sangat tinggi, memperlihatkan gejala kelumpuhan sistem syarat dan kekejangan. Penelitian lain menunjukkan bahwa tikus yang dipajan NO sampai 2500 ppm akan hilang kesadarannya setelah 6-7 menit, tetapi jika kemudian diberi udara segar akan sembuh kembali setelah 4–6 menit. Tetapi jika pemajanan NO pada kadar tersebut berlangsung selama 12 menit, pengaruhnya tidak dapat dihilangkan kembali, dan semua tikus yang diuji akan mati. NO2 bersifat racun terutama terhadap paru. Kadar NO2 yang lebih tinggi dari 100 ppm dapat mematikan sebagian besar binatang percobaan dan 90% dari kematian tersebut disebabkan oleh gejala pembengkakan paru (edema pulmonari). Kadar NO2 sebesar 800 ppm akan mengakibatkan 100% kematian pada binatang-binatang yang diuji dalam waktu 29 menit atau kurang. Pemajanan NO2 dengan kadar 5 ppm selama 10 menit terhadap manusia mengakibatkan kesulitan dalam bernapas (Darmono, 2006).
2. Lingkungan
Proses oksidasi di atmosfer mengakibatkan gas-gas tersebut berubah menjadi H2SO4 dan HNO3 meningkatkan keasaman air hujan.
Smog fotokimia timbul sebagai akibat terjadi reaksi fotokimia antara pencemar-pencemar udara, khususnya pencemar HC dan NOx dengan bantuan sinar matahari.
3. Tumbuhan
Udara yang tercemar oleh gas nitrogen dioksida tidak hanya berbahaya bagi manusia dan hewan saja, tetapi juga berbahaya bagi kehidupan tanaman. Pengaruh gas NO2 pada tanaman antara lain timbulnya bintik-bintik pada permukaan daun. Pada konsentrasi lebih tinggi, gas tersebut dapat menyebabkan nekrosis atau kerusakan pada jaringan daun, dalam keadaan seperti ini daun tidak dapat berfungsi sempurna.
Udara yang tercemar oleh gas nitrogen dioksida tidak hanya berbahaya bagi manusia dan hewan saja, tetapi juga berbahaya bagi kehidupan tanaman. Pengaruh gas NO2 pada tanaman antara lain timbulnya bintik-bintik pada permukaan daun. Pada konsentrasi lebih tinggi, gas tersebut dapat menyebabkan nekrosis atau kerusakan pada jaringan daun, dalam keadaan seperti ini daun tidak dapat berfungsi sempurna.
Pencegahan dan Pengendalian
Pencegahan pencemaran udara pada(Husein,1993).
1. Sumber Bergerak
Apabila kadar NO2, kadar oksidan, khlorin, dan timah dalam udara ambien telah melebihi baku mutu dengan rata-rata waktu pengukuran 24 jam maka untuk mencegah dampak kesehatan, dilakukan upaya-upaya :
1. Sumber Bergerak
- Merawat mesin kendaraan bermotor agar tetap berfungsi baik
- Melakukan pengujian emisi dan KIR kendaraan secara berkala
- Memasang filter pada knalpot
- Memasang scruber pada cerobong asap.
- Merawat mesin industri agar tetap baik dan lakukan pengujian secara berkala.
- Menggunakan bahan bakar minyak atau batu bara dengan kadar Sulfur, CO rendah.
- Memodifikasi pada proses pembakaran.
- Pembersihan ruangan dengan sistem basah.
Apabila kadar NO2, kadar oksidan, khlorin, dan timah dalam udara ambien telah melebihi baku mutu dengan rata-rata waktu pengukuran 24 jam maka untuk mencegah dampak kesehatan, dilakukan upaya-upaya :
- Menggunakan alat pelindung diri (APD), seperti masker gas.
- Mengurangi aktifitas diluar rumah.
Upaya Pemerintah Pusat
Adapun upaya-upaya yang dilakukan oleh pemeritah pusat untuk mencegah dan mengendalikan pencemaran udara antara lain:
1. Penetapan peraturan perundang-undangan yang terkait dengan pencemaran udara seperti Peraturan Pemerintah (PP) Nomor 41 Tahun 1999 tentang Pengendalian Pencemaran Udara.
2. Penentuan pengelola pengawasan dan penanggungjawab pengendalian pencemaran udara serta dampaknya, yaitu:
1. Penetapan peraturan perundang-undangan yang terkait dengan pencemaran udara seperti Peraturan Pemerintah (PP) Nomor 41 Tahun 1999 tentang Pengendalian Pencemaran Udara.
2. Penentuan pengelola pengawasan dan penanggungjawab pengendalian pencemaran udara serta dampaknya, yaitu:
- Kementerian Negara Lingkungan Hidup bertanggungjawab terhadap regulasi emisi dan pemantauan dampak lingkungan yang terjadi;
- Departemen Energi dan Sumber Daya Mineral bertanggungjawab terhadap pengawasan dan pengendali mutu bahan bakar;
- Departemen Perindustrian bertanggungjawab mengawasi produk komponen kendaraan yang ramah lingkungan dan mengawasi dan sertifikasi bengkel dalam rangka meningkatkan kualitas udara di perkotaan;
- Departemen Perhubungan bertanggungjawab pengujian tipe untuk kendaraan bermotor produksi baru termasuk uji emisi gas buang dan pengadaan dan pemasangan converter kita.
- Pemerintah Daerah bertanggungjawab terhadap pengujian kendaraan bermotor yang sedang berjalan.
Sumber
http://cha2in-chemistry09.blogspot.com/2012/11/pencemaran-nox-pada-gas-udara.html. Diunduh pada tanggal 19 Februari 2013.
http://www.dirgantara-lapan.or.id/jizonpolud/htm/nox.htm. Diunduh pada tanggal 19 Februari 2013.
http://www.dirgantara-lapan.or.id/jizonpolud/htm/nox.htm. Diunduh pada tanggal 19 Februari 2013.